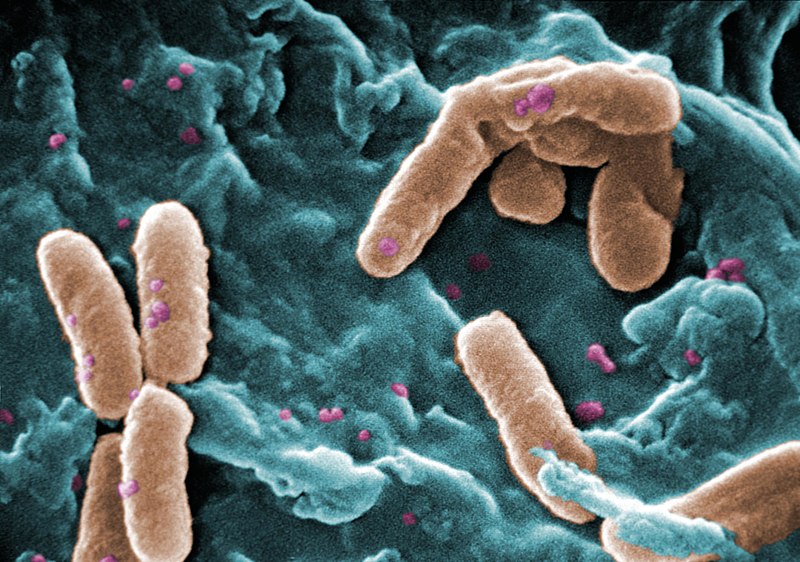
 Wir haben ein Problem und es wird schlimmer – multiresistente Bakterien. In den Nachrichten hört man immer wieder davon, sie werden „multiresistente Keime/ Erreger“, manchmal auch „multiresistente Krankenhauskeime“ genannt. Dabei handelt es sich um Bakterien, die nicht mehr durch Antibiotika bekämpft werden können. Solche Bakterien können sich zum Beispiel in offenen Wunden ansiedeln und deren Heilung verhindern. Auch unter Erregern von Tuberkulose, Durchfall und Lungenentzündung sind bereits multiresistente Erreger (MRE) aufgetaucht. Besonders häufig hört man dieser Tage von Pseudomonas aeruginosa, einem Krankenhauskeim, der 10 % aller Krankenhausinfektionen verursacht. Dieses Stäbchenbakterium ruft unter anderem Harnwegsinfektionen, Dickdarm- oder Hirnhautentzündungen hervor. Besonders Menschen mit schwachem Immunsystem, z.B. Kinder und ältere Leute oder Menschen mit Vorerkrankungen sind anfällig für die Infektion mit einem solchen MRE. Doch wie konnte es dazu kommen, dass Bakterien immun sind gegen fast jedes bekannte Antibiotikum? Und was können wir auf lange Sicht dagegen tun?
Wir haben ein Problem und es wird schlimmer – multiresistente Bakterien. In den Nachrichten hört man immer wieder davon, sie werden „multiresistente Keime/ Erreger“, manchmal auch „multiresistente Krankenhauskeime“ genannt. Dabei handelt es sich um Bakterien, die nicht mehr durch Antibiotika bekämpft werden können. Solche Bakterien können sich zum Beispiel in offenen Wunden ansiedeln und deren Heilung verhindern. Auch unter Erregern von Tuberkulose, Durchfall und Lungenentzündung sind bereits multiresistente Erreger (MRE) aufgetaucht. Besonders häufig hört man dieser Tage von Pseudomonas aeruginosa, einem Krankenhauskeim, der 10 % aller Krankenhausinfektionen verursacht. Dieses Stäbchenbakterium ruft unter anderem Harnwegsinfektionen, Dickdarm- oder Hirnhautentzündungen hervor. Besonders Menschen mit schwachem Immunsystem, z.B. Kinder und ältere Leute oder Menschen mit Vorerkrankungen sind anfällig für die Infektion mit einem solchen MRE. Doch wie konnte es dazu kommen, dass Bakterien immun sind gegen fast jedes bekannte Antibiotikum? Und was können wir auf lange Sicht dagegen tun?
Antibiotika (die Einzahl lautet übrigens „Antibiotikum“) sind Stoffe, die Bakterien (und nur Bakterien – keine Viren!) abtöten können. Sie kommen vielfach in der Natur vor, da sie meistens von Bakterien oder Pilzen produziert und ausgeschieden werden. Die Bakterien und Pilze nutzen sie, um andere Mikroorganismen in ihrer Umgebung in Schach zu halten und möglichst viele Nahrungsquellen für sich zu behalten. Das allererste Antibiotikum, das von einem Wissenschaftler entdeckt wurde, war das Penicillin. Es wird von einem Schimmelpilz namens Penicillium hergestellt. Bereits 1893 konnte Bartolomeo Gosio Penicillin aus dem Pilz gewinnen. Seine Ergebnisse blieben jedoch unbekannt. 1897 veröffentlichte der französische Militärarzt Ernest Duchnese seine Doktorarbeit, in der er beschrieb, dass die Stallknechte im Militärhospital die Sättel der Pferde in einem dunkeln, feuchten Raum aufbewahrten, um die Bildung von Schimmel auf den Sätteln zu fördern. Auf die Frage, warum sie dies täten, antworteten die Stallknechte, dass die wunden Stellen auf den Rücken der Pferde dadurch besser heilten. Duchnese injizierte daraufhin einem Meerschweinchen, das er zuvor mit Typhus infiziert hatte, den Schimmelpilz. Das Meerschweinchen wurde vollkommen gesund.
Seit der Entdeckung des Penicillins wurde viele andere Antibiotika gefunden und jahrzehntelang erfolgreich zur Krankheitsbekämpfung eingesetzt. Doch damit begann auch das Problem. Die DNA von Bakterien verändert sich ständig durch zufällig auftretende Mutationen. Dabei kann es passieren, dass ein Gen entsteht, dass das Bakterium resistent macht gegen ein bestimmtes Antibiotikum. Wenn dieses Bakterium nun zum Beispiel an den Mandeln eines Patienten sitzt, der dieses Antibiotikum einnimmt, wird es nicht sterben. Stattdessen kann es sich rasant vermehren und so den Patienten zu einer Quelle eines resistenten Erregers machen. Von ihm aus kann es sich auf andere Menschen verbreiten.
Auch die Unzuverlässige Einnahme von Antibiotika kann resistente Keime erzeugen. Wenn man frühzeitig aufhört, das verschriebene Antibiotikum einzunehmen, weil man sich besser fühlt, wurden womöglich nicht alle Keime abgetötet. Die noch lebenden Keime können dann Resistenzen entwickeln.
Ein bedeutender – vielleicht der bedeutendste – Faktor heutzutage ist die massenhafte Verabreichung von Antibiotika an Tiere in Schlachthöfen. Damit will man verhindern, dass die Tiere krank werden. Würde ein Tier in Massenhaltung krank, könnte sich die Krankheit durch den engen Kontakt mit seinen Artgenossen rasend schnell in der ganzen Anlage verbreiten. Das will man verhindern und so gibt man extrem hohe Dosen Antibiotika. Wenn wir das Fleisch dieser Tiere essen, nehmen wir die Antibiotika auf und erschaffen dadurch in unserem Körper eine Brutstätte für Keime, die sich nun anpassen und Resistenzen entwickeln müssen.
Was kann die Wissenschaft tun, um diese verheerende Entwicklung aufzuhalten? Eine Abschaffung der Massentierhaltung wäre natürlich wünschenswert, würde aber lange dauern – zu lange. Also müssen schnell neue Antibiotika her. Da man diese aus Bakterien in der Natur gewinnt, könnte man einfach neue Bakterien suchen. Das hat man auch getan. Und festgestellt, dass sie nur Antibiotika herstellen, die schon auf dem Markt sind.
Man nimmt sogar an, dass man alle Bakterien, die sich im Labor kultivieren lassen, bereits kennt. Doch das sind nur etwa 1 % aller bekannten Bakterien! Die restlichen 99 %, die „dunkle Seite“, lassen sich nicht im Labor halten. Wenn man sie auf einem Nährboden versucht zu kultivieren, sterben sie. Was tun? Nun, wenn der Prophet nicht zum Berg kommt, muss der Berg eben zum Propheten kommen, nicht wahr! Die Mikrobiologen Slava Epstein und Kim Lewis haben eine Apparatur erfunden, mit der man Bakterien direkt in der Natur kultivieren kann. Kleine Kammern, die mit einer porösen Membran abgedeckt werden, werden in den Boden eingelassen. Die Poren in der Membran sind so klein, dass nur Bakterien hindurchpassen. Bakterien aus dem Boden können in die Kammern einwandern und dort wachsen. Nach etwa zwei Wochen „erntet“ man die Bakterien und untersucht, ob sie unbekannte Antibiotika produzieren.
Einige kleine Erfolge gab es bereits. Zwei neue Antibiotika namens lassomycin und Teixobactin wurden gefunden. Beide wirken gegen Tuberkulosebakterien und kein untersuchtes Bakterium zeigte Resistenz gegen Teixobactin.
Es besteht also Hoffnung. Dennoch geht die Suche sehr langsam voran und niemand kann vorhersagen, wie schnell neue resistente Keime auftauchen, denen auch die neuen Antbiotika nichts mehr ausmachen. Wer weiß, vielleicht brauchen wir eine ganz neue Herangehensweise in der Bekämpfung von bakteriellen Krankheiten. Ich bin neugierig, was den Wissenschaftlern einfällt und halte euch auf dem Laufenden!
